CRISPR技术是一种革命性的基因编辑工具,它为科学家们提供了一种精确的方法来操纵DNA序列。在诱导多能干细胞(iPSCs)的研究中,CRISPR技术的作用日益凸显。通过编辑iPSCs,研究人员能够更好地理解人类疾病的机制,并为疾病的治疗提供新的思路。

本篇文章主要讨论了一种名为柔性分选的细胞分选方法,该方法可以加速生成基因编辑的诱导多能干细胞(iPSCs)。研究人员使用CRISPR技术对iPSCs进行基因编辑,以用于体外疾病模型研究。通过使用Gentle Sorting方法,研究人员能够更快地筛选和分离编辑过的细胞,从而提高了iPSCs的生成效率。这项研究由Baylor College of Medicine和NanoCellect Biomedical, Inc.的科学家共同完成。
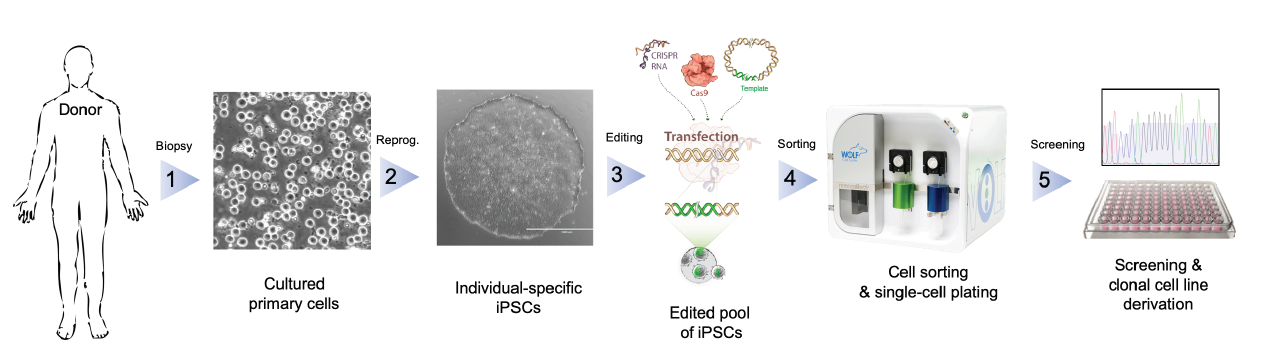
研究过程中,研究人员发现,在获取患者细胞并诱导其成为iPSCs的环节中,通过巧妙运用特定的标记物,我们能够更有效地富集目标细胞,进而优化分化过程。最终,精确选择和培育经过CRISPR编辑的单个细胞,极大地提升了整个工作流程的效率。值得一提的是,在整个操作过程中,研究人员始终采用低压力分选技术,旨在最大程度地减少对这些脆弱细胞的潜在伤害。这种技术不仅确保了细胞的完整性,还极大地提升了实验的成功率。
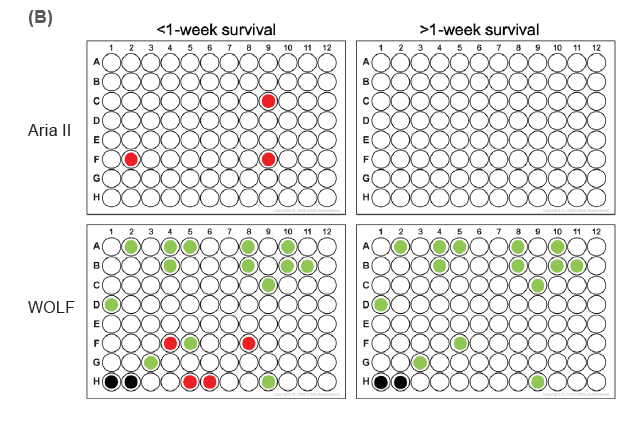
在细胞分选环节,WOLF单细胞柔性分选系统相较于传统的BD FACS Aria II展现出了显著的优势。它运用微流控技术,通过低压力和无液滴/气溶胶机制,极大地降低了剪切应力和压力,从而显著提高了细胞的存活率。实验数据表明,使用WOLF细胞分选系统进行单细胞分选后,细胞在一周后仍能保持较高的存活率,而传统方法则无法达到这一效果。
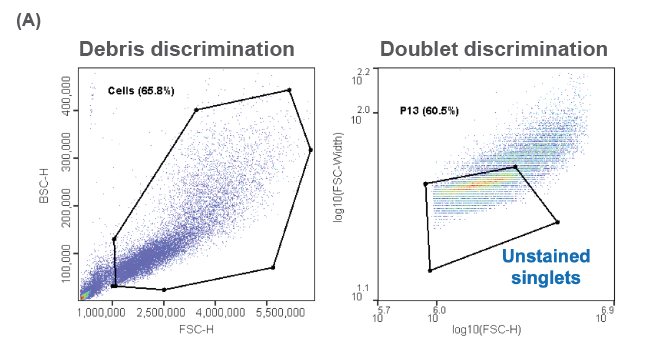
不仅如此,WOLF单细胞柔性分选系统还具备高度的可选择性,它可以根据荧光检测精准地选择和分选细胞,如识别GFP表达和荧光活力染料标记的细胞。同时,它还能利用特定的染料排除死细胞,进一步提高了实验的准确性和可靠性。此外,其内置的软件功能使得筛选和分选单个细胞变得更加便捷,有效减少了黏连细胞的产生,这对于单细胞克隆研究具有重要意义。
综上所述,采用低压力分选技术能够显著优化诱导多能干细胞(iPSCs)的生成工作流程,从而加速基因编辑iPSCs的产生。通过精心选择筛选标准,可以有效分离多能干细胞与未经重编程的细胞。同时,利用特定标记物富集目标细胞,能够进一步优化分化过程。在整个过程中,WOLF单细胞柔性分选系统的应用不仅提高了实验效率,还确保了细胞的健康和完整性。
WOLF作为一款可用于分析、分选和分配的多功能细胞分选仪,紧凑且易于使用,可用于任何规模的基因编辑实验室。它不仅能帮助科研人员减少工作流程中的重复工作与所需耗时,还可确保分配到孔板中的细胞具备更高的存活率。同腾睿杰(上海)生物科技有限公司作为Nanocellect中国南区总代理商,为您提供优质的售前售后服务。
联系电话:021-50826962
联系邮箱:sales@ttbiotech.com




